摘要:目的:探讨血清铁蛋白在肠衰竭相关性肝病中的诊断价值。方法:回顾性分析2019年1月至2022年12月南京大学附属金陵医院普通外科收治的106例成人短肠综合征病人的临床资料,通过线性回归确定
目的:探讨血清铁蛋白在肠衰竭相关性肝病中的诊断价值。方法:回顾性分析2019年1月至2022年12月南京大学附属金陵医院普通外科收治的106例成人短肠综合征病人的临床资料,通过线性回归确定血清铁蛋白与肝脏酶谱的相关性,采用多因素Logistic回归分析筛选肝损伤的潜在危险因素并建立肝纤维化预测模型,计算曲线下面积评估模型准确性。结果:55例(51.9%)病人血清铁蛋白(SF)升高;线性回归分析显示血清铁蛋白与ALT(r=0.427,P<0.001)、ALP(r=0.365,P<0.001)及γ-GT(r=0.423,P<0.001)呈正相关;单因素Logistic回归分析显示血清铁蛋白水平越高,差异越显著(SF>ULN,P=0.033;SF>1.5×ULN,P=0.018;SF>2.5×ULN,P=0.006);多因素Logistic回归分析显示,PN依赖(OR=3.366,P=0.017)、血清铁蛋白>2.5×ULN(OR=3.292,P=0.014)是肠衰竭相关性肝病-肝纤维化的独立危险因素;受试者工作曲线(ROC)显示曲线下面积为74.8%(95%CI:0.652~0.844)。结论:血清铁蛋白可作为可靠的临床生物标志物,帮助识别肠衰竭相关性肝病。
关键词:血清铁蛋白;肠外营养;肠衰竭;肝纤维化
论文《血清铁蛋白可识别肠衰竭相关性肝病》发表在《肠外与肠内营养》,版权归《肠外与肠内营养》所有。本文来自网络平台,仅供参考。
一、引言
慢性肠衰竭(chronic intestinal failure, CIF)指肠道功能持续降低,无法满足营养素、水和电解质的吸收需求,需静脉补充维持健康和生长。肠外营养(parenteral nutrition, PN)是挽救肠衰竭病人生命的关键措施,但长期接受PN的病人易出现肝脏损伤,发病率达15%~40%,其确切机制尚未明确。
肠衰竭相关性肝病(intestinal failure-associated liver disease, IFALD)是排除其他原发性肝病后,长期PN治疗的肠衰竭病人出现的一系列肝病,包括胆汁淤积、脂肪性肝炎、肝纤维化及肝硬化。临床表现从血清转氨酶和γ-谷氨酰转肽酶(γ-GT)轻度升高,到严重胆汁淤积性肝损伤、门脉高压甚至肝衰竭,主要依据肝酶谱浓度变化判断。这些指标在PN治疗后2~4周显著升高,停止PN后肝功能可改善,但肝纤维化和脂肪变性难以完全逆转。
IFALD后期肝细胞大量死亡引发炎症反应,导致胆酶分离和纤维化形成,且难以逆转,因此早期识别IFALD-肝纤维化对改善病人预后至关重要。目前临床上缺乏理想的预测指标,病理活检的有创性限制了其应用,已有研究探索γ-GT、瓜氨酸和肝脏硬度的联合诊断价值,其ROC值高于0.90。临床实践中发现,肠衰竭病人肝功能异常时常伴有血清铁蛋白升高。
血清铁蛋白反映体内铁储存情况,是氧化应激及自由铁负荷的特异性标记物,其异常与高胆固醇血症、急性胰腺炎、脂肪性肝炎、肝纤维化及癌症相关。但血清铁蛋白与肝脏疾病的确切联系尚不明确,本研究旨在探讨血清铁蛋白水平与肝功能异常的相关性,明确其在IFALD-肝纤维化中的诊断价值。
二、资料和方法
(一)研究对象
回顾性收集2019年1月至2022年12月南京大学附属金陵医院普通外科住院的成人短肠综合征(short bowel syndrome, SBS)病人106例,其中男78例,女28例,年龄18~80岁,平均年龄(53.5±14.0)岁。
纳入标准:①年龄18~80岁;②短肠综合征病人接受PN治疗至少6个月,剩余小肠长度小于200cm(参考2016年欧洲临床营养与代谢协会(ESPEN)肠衰竭指南);③每例病人均接受肝脏二维剪切波弹性成像或腹部CT检查。
排除标准:①本身患有其他肝病(病毒性肝炎、酒精性/非酒精性肝病、胆道闭锁、原发性胆管炎等);②近5年内有恶性肿瘤病史;③有精神疾患或不能合作者;④妊娠或哺乳期妇女;⑤严重肾功能不全(肌酐值高于正常上限2倍);⑥已入选其他临床研究或曾入选本研究的病人。本研究为回顾性研究,豁免知情同意书。
(二)研究方法
1. 分组方法
根据病人入院第一次血清铁蛋白水平,分为血清铁蛋白升高组(>正常值上限(upper limit of normal, ULN)1.5倍)和血清铁蛋白正常组(≤ULN×1.5倍)。
2. 观察指标
收集病人一般临床资料,包括年龄、性别、身高、体质量、BMI、病史(手术史、剩余肠管情况、短肠综合征类型等)、是否存在PN依赖(患病至最后一次随访期间使用PN维持,且使用频次不小于2次/周)、NRS 2002评分、短肠综合征病程及伴随疾病(高血压、糖尿病等)。采集入院第一次的血常规、肝酶谱(谷丙转氨酶(ALT)、谷草转氨酶(AST)、碱性磷酸酶(ALP)、谷氨酰转移酶(γ-GT))、胆红素(总胆红素、直接胆红素)、胆固醇、血清铁蛋白、电解质、甘油三酯等指标。
3. 判定方法
采用二维剪切波弹性成像(2D-SWE)评估肝纤维化,该方法被中华医学会超声学分会推荐为无创评估肝纤维化的重要手段。使用C1-5/60腹凸探头(Angiodin-Sono/P-Ultra,俄罗斯BIOSS公司)获取信号测量肝脏硬度,在肝包膜下1~2cm测量,避开血管和胆管,对每位病人测量三次取平均值,肝脏硬度值>6.5kPa时评估为纤维化。
4. 统计学方法
应用SPSS 23.0软件进行统计分析。符合正态分布的计量资料以(x̄±s)表示,组间比较采用t检验;非正态分布的计量资料以中位数和四分位数间距表示,组间比较采用Wilcoxon W检验;计数资料以例和百分比表示,组间比较采用χ²检验。采用Pearson相关分析血清铁蛋白与肝脏酶谱的相关性,使用单因素和多因素Logistic回归探究IFALD-纤维化的危险因素,通过受试者操作特征曲线(ROC)评估临床指标的诊断价值,以P<0.05为差异有统计学意义。
三、结果
(一)一般资料
两组病人在性别、年龄、身高、体质量、BMI、NRS 2002评分、短肠综合征病程及伴随疾病(高血压、糖尿病)等方面无显著性差异(P>0.05)。两组在PN使用时间上存在显著差异(P=0.033),PN依赖情况也具有显著差异(P=0.022):32例(30.2%)病人存在PN依赖,其中铁蛋白升高组22例(40.0%),正常组10例(19.6%)。总胆红素、直接胆红素、ALT、AST、ALP和γ-GT在两组中均存在明显差异(P<0.05)。此外,铁蛋白升高组胆固醇(3.0ng/mL vs 2.5ng/mL)和炎症指标C反应蛋白(18.7mg/L vs 1.0mg/L)均明显高于正常组(P<0.05)。
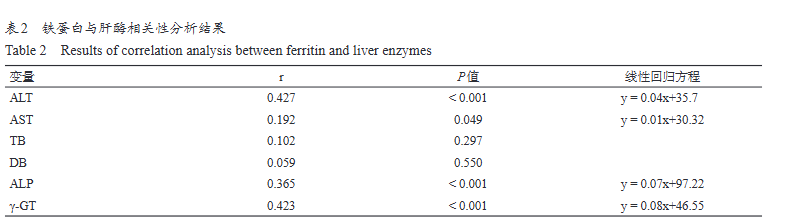
(二)血清铁蛋白与肝功能指标相关性分析
相关性分析结果显示,血清铁蛋白与ALT、ALP以及γ-GT呈显著正相关(P<0.001),与AST呈弱正相关(r=0.192,P=0.049),与总胆红素、直接胆红素相关性不显著(P>0.05)。
(三)肠道解剖情况及病因分析
两组在剩余小肠长度方面存在显著差异(P<0.001),铁蛋白升高组平均小肠长度为77.6cm,正常组为110.7cm。在短肠综合征的类型、剩余肠管类型、回盲瓣完整性、结肠完整性及短肠病因方面,两组无显著性差异(P>0.05)。
(四)Logistic回归分析肝纤维化发生的危险因素
单因素Logistic回归发现,PN依赖(OR=4.140,P=0.002)是肝纤维化的危险因素,年龄无统计学意义(P=0.148)。不同血清铁蛋白临界值分组均显示显著差异,且数值越高差异越明显(SF>ULN,P=0.033;SF>1.5×ULN,P=0.018;SF>2.5×ULN,P=0.006)。多因素Logistic回归分析显示,PN依赖(OR=3.366,95%CI:1.244~9.107,P=0.017)、血清铁蛋白>2.5×ULN(OR=3.292,95%CI:1.279~8.475,P=0.014)是IFALD-肝纤维化的独立危险因素。基于这两个指标建立的回归模型,ROC曲线下面积为74.8%(95%CI:0.652~0.844),可有效预测IFALD-肝纤维化的发生。
四、讨论
本研究发现,血清铁蛋白与肠衰竭病人的ALT、AST、ALP、γ-GT具有相关性,血清铁蛋白>2.5×ULN和PN依赖是IFALD-肝纤维化的独立危险因素,基于这两个指标建立的模型ROC曲线下面积为0.748,表明血清铁蛋白可作为可靠的临床生物标志物,帮助识别IFALD。
血清铁蛋白是氧化应激及自由铁负荷的特异性标记物,研究表明其可能与胰岛素抵抗相关,而胰岛素抵抗是肝细胞脂肪变性的主要原因。此外,体内的铁可通过催化芬顿反应促进活性氧产生,降低一氧化氮生物利用度,破坏肝窦内皮细胞功能,加剧组织炎症。铁蛋白是非酒精性脂肪性肝病(NAFLD)的独立危险因素,肝脏铁沉积可能通过介导细胞损伤,加速NAFLD的纤维化进展。
有研究报道血清铁蛋白水平随年龄升高而增高,老年人群铁蛋白升高可能与炎症相关,但本研究未证实这一结论,可能与IFALD更多与肠外营养应用及代谢相关有关。此前研究表明BMI与脂肪肝易感基因风险变异存在交互作用,但本研究中BMI无显著影响,可能与短肠综合征病人本身存在营养不良、BMI相对较低有关。
肝病的发生多与代谢异常相关,肝脏作为机体代谢最旺盛的器官,参与糖脂及药物代谢。胰岛素抵抗被证实是NAFLD的独立危险因素,糖尿病也易导致肝功能紊乱,但本研究未观察到这一趋势,可能与病人患病前糖尿病史占比低(5.7%),且住院期间血糖被严格监测有关。
波士顿的一项研究发现,126名肠衰竭病人肝活检发生肝硬化的概率为18%,且与PN使用时间显著相关。由于PN病人通常缺乏肠内喂养刺激,肠腔激动剂对肠上皮细胞受体的激活减少,可能干扰正常肠-肝循环,造成肝功能异常甚至不可逆肝损伤。本研究也证实PN依赖是肝纤维化的危险因素,因此合理使用肠外营养对避免肝损伤进展至关重要。
本研究存在一定局限性:第一,缺乏病人肝穿刺活检病理结果,可能低估肝纤维化实际发生例数,且未对血清铁蛋白进行动态监测,无法评估其与PN时间的关系;第二,为小样本单中心回顾性研究,结果可能存在偏倚,后续需纳入更多病例,探索IFALD-肝纤维化的有效生物标志物并建立稳定模型;第三,结果仍需多中心大样本前瞻性研究进一步验证。
综上,血清铁蛋白水平与肠衰竭病人的肝酶指标具有相关性,血清铁蛋白>2.5×ULN和PN依赖是IFALD-肝纤维化的独立危险因素,血清铁蛋白可作为协助诊断IFALD的可靠生物标志物。
参考文献
[1] Pironi L, Arends J, Baxter J, et al. ESPEN endorsed recommendations. Definition and classification of intestinal failure in adults[J]. Clin Nutr, 2015, 34(2):171-180.
[2] Zafirovska M, Zafirovski A, Rotovnik Kozjek N. Current insights regarding intestinal failure-associated liver disease (IFALD): A narrative review[J]. Nutrients, 2023, 15(14):3169.
[3] Mutanen A, Lohi J, Heikkilä P, et al. Persistent abnormal liver fibrosis after weaning off parenteral nutrition in pediatric intestinal failure[J]. Hepatology, 2013, 58(2):729-738.
[4] Lauriti G, Zani A, Aufieri R, et al. Incidence, prevention, and treatment of parenteral nutrition-associated cholestasis and intestinal failure-associated liver disease in infants and children: A systematic review[J]. JPEN J Parenter Enteral Nutr, 2014, 38(1):70-85.
[5] Robinson DT, Ehrenkranz RA. Parenteral nutrition-associated cholestasis in small for gestational age infants[J]. J Pediatr, 2008, 152(1):59-62.
[6] Mutanen A, Lohi J, Merras-Salmio L, et al. Prediction, identification and progression of histopathological liver disease activity in children with intestinal failure[J]. J Hepatol, 2021, 74(3):593-602.
[7] Preziosi ME, Singh S, Valore EV, et al. Mice lacking liver-specific β-catenin develop steatohepatitis and fibrosis after iron overload[J]. J Hepatol, 2017, 67(2):360-369.
[8] 许尧, 袁晨晨, 马孝杰, 等. 血清铁与急性胰腺炎病人预后的相关性研究[J]. 肠外与肠内营养, 2023, 30(1):25-30.
[9] 梁萍, 郑荣琴. 二维剪切波弹性成像评估慢性乙型肝炎肝纤维化临床应用指南[J]. 临床肝胆病杂志, 2018, 34(2):255-261.
[10] Tarasova OI, Kuhareva EI, Krasnitskaya SK, et al. Evaluation of the effectiveness of ultrasound shear elastography and liver steatometry[J]. Ter Arkh, 2020, 92(4):17-22.
[11] Jung JY, Shim JJ, Park SK, et al. Serum ferritin level is associated with liver steatosis and fibrosis in Korean general population[J]. Hepatol Int, 2019, 13(2):222-233.
[12] Letelier ME, Sánchez-Jofré S, Peredo-Silva L, et al. Mechanisms underlying iron and copper ions toxicity in biological systems: Pro-oxidant activity and protein-binding effects[J]. Chem Biol Interact, 2010, 188(1):220-227.
[13] Manousou P, Kalambokis G, Grillo F, et al. Serum ferritin is a discriminant marker for both fibrosis and inflammation in histologically proven non-alcoholic fatty liver disease patients[J]. Liver Int, 2011, 31(5):730-739.
[14] Yao J, Dai Y, Zhang J, et al. Association between serum ferritin level and nonalcoholic fatty liver disease in a non-obese Chinese population: A cross-sectional study[J]. Clin Lab, 2019, 65(6).
[15] Mörwald K, Aigner E, Bergsten P, et al. Serum ferritin correlates with liver fat in male adolescents with obesity[J]. Front Endocrinol (Lausanne), 2020, 11:340.
[16] Tsuboi H, Segawa S, Yagishita M, et al. Activation mechanisms of monocytes/macrophages in adult-onset still disease[J]. Front Immunol, 2022, 13:953730.
[17] Kowdley KV, Belt P, Wilson LA, et al. Serum ferritin is an independent predictor of histologic severity and advanced fibrosis in patients with nonalcoholic fatty liver disease[J]. Hepatology, 2012, 55(1):77-85.
[18] Ajmera V, Wang N, Xu H, et al. Longitudinal association between overweight years, polygenic risk and NAFLD, significant fibrosis and cirrhosis[J]. Aliment Pharmacol Ther, 2023, 57(10):1143-1150.
[19] Sohn W, Kwon HJ, Chang Y, et al. Liver fibrosis in Asians with metabolic dysfunction-associated fatty liver disease[J]. Clin Gastroenterol Hepatol, 2022, 20(5):e1135-e1148.
[20] Fullerton BS, Sparks EA, Hall AM, et al. Enteral autonomy, cirrhosis, and long term transplant-free survival in pediatric intestinal failure patients[J]. J Pediatr Surg, 2016, 51(1):96-100.
[21] Villalona G, Price A, Blomenkamp K, et al. No gut no gain! Enteral bile acid treatment preserves gut growth but not parenteral nutrition-associated liver injury in a novel extensive short bowel animal model[J]. JPEN J Parenter Enteral Nutr, 2018, 42(8):1238-1251.
[22] 刘坤慧, 颜伟慧, 蔡威. 肠屏障功能与肠外营养相关肝损伤关系研究进展[J]. 肠外与肠内营养, 2022, 29(6):370-374.





