摘要:为探究2,4-表油菜素内酯(EBL)对谷子萌发的影响及其生理机制,从而为提高谷子耐盐性提供理论支持,研究10^-10、10^-9、10^-8、10^-7 mol/L 2,4-表油菜素内酯浸种处理对0、50、100、150、200、250、300 m
为探究2,4-表油菜素内酯(EBL)对谷子萌发的影响及其生理机制,从而为提高谷子耐盐性提供理论支持,研究10^-10、10^-9、10^-8、10^-7 mol/L 2,4-表油菜素内酯浸种处理对0、50、100、150、200、250、300 mmol/L NaCl胁迫下的谷子萌发和生长的影响。结果表明,随着NaCl胁迫浓度的升高,每组EBL浸种处理均降低了谷子发芽势、发芽率、胚根长、胚轴长及萌发后的含水量。在0、50、100mmol/L的低浓度NaCl胁迫下,每组EBL浸种处理对谷子萌发情况均无显著影响;在150、200mmol/L的中等浓度NaCl胁迫下,不同EBL浸种处理会不同程度地影响谷子萌发情况,在所有处理组中,10^-9 mol/L EBL对200mmol/L NaCl胁迫下谷子的萌发效果影响最显著(P<0.05);在250、300 mmol/L的高浓度NaCl胁迫下,每组EBL浸种处理促进谷子萌发的效果均不明显。在200 mmol/L NaCl处理下10^-9 mol/L EBL浸种处理组中,萌发谷子体内的丙二醛(MDA)含量相比不施用EBL的对照组显著降低(P<0.05),超氧化物歧化酶(SOD)、过氧化物酶(POD)活性相比不施用EBL的对照组显著升高(P<0.05)。
关键词: 谷子; 油菜素内酯; 盐胁迫; 种子萌发; 生理机制
论文《油菜素内酯浸种对盐胁迫谷子萌发的影响及其生理机制》发表在《江苏农业科学》,版权归《江苏农业科学》所有。本文来自网络平台,仅供参考。
正文
引言
土地盐渍化能使得作物生长发育受到严重影响,是全球关注的环境问题之一,已成为干旱、半干旱地区农业发展的主要威胁。目前,全世界盐渍化土壤面积已经超过10亿hm²,预计到2050年,全球有50%的耕地发生盐渍化[1]。我国盐渍化土壤分布广泛,总面积位居世界第3,属于我国主要的中低产土壤类型之一,在很大程度上限制了我国农业的生产与发展。谷子(Setaria italica)是狗尾草属一年生草本植物,为五谷杂粮之首,谷子经去壳处理后,成为日常生活中必不可少的小米。小米不仅有保健身体的作用,还有帮助食用者安神的作用,食用价值较高,因此,人们对于小米的需求量较大[2]。
另外,谷子除了具有较高的营养价值外,还具有粮饲兼用、抗旱耐瘠薄、适应性强等特点[3],是一种典型的环境友好型作物[4]。虽然谷子的耐盐性高于水稻、玉米等作物,但是随着我国土壤盐渍化问题日益严重,对我国谷子的萌发、生长都造成较大的不利影响[5]。面对日益扩大的盐碱地面积和巨大的粮食需求,提高盐渍地上谷子的萌发率显得尤为重要。
油菜素内酯(brassinolide, BR)被列为第六大植物激素,在植物的花粉、种子及根、茎、叶中都有分布[6],BR中芸苔素内酯(BL)、2,4-表油菜素内酯(EBL)和2,8-高油菜素内酯(HBL)是活性较高的3种,油菜素内酯作为一种新型、高效的植物激素,在植物的生长发育过程以及植物响应生物、非生物胁迫过程中发挥着不可或缺的作用,它能够通过促进植物光合作用和抗逆性来促进植物的生长发育,影响果实产量和品质形成[7]。
权梦萍等研究油菜素内酯对非生物逆境胁迫下植物生长的影响,发现油菜素内酯可以通过改善植物的相关生理系统来提高植物对非生物胁迫的耐受性,促进植物生长[8]。有研究者分析了油菜素内酯对盐胁迫下黑麦草、菜豆、绿豆和水稻种子萌发及生理的影响,发现外源BR处理可以提高黑麦草种子的发芽率、发芽势,可以增强相应酶活性[9-12]。吕宗环等使用不同浓度的NaCl溶液对10份谷子进行处理,明确了适合谷子萌发期抗盐鉴定的NaCl浓度为180 mmol/L[13]。张永芳等设置了5个碳酸钠浓度对4个谷子品种进行盐胁迫处理,结果表明,低浓度的碳酸钠能够促进谷子萌发,但是随着其浓度增加,萌发指标会逐渐降低[14]。Nie等研究2,4-表油菜素内酯对碳酸氢钠胁迫黄瓜种子萌发的改善作用,发现EBL处理后显著提高了超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、过氧化物酶(POD)的活性,缓解盐胁迫引起的氧化损伤,显著抵消对种子萌发的抑制作用[15]。Chakma等用2,4-表油菜素内酯(EBL)单独处理或将其与其他激素联合处理棉花种子进行萌发试验,结果表明,EBL在有或无盐胁迫的条件下都能促进种子萌发,而其他激素在胁迫下均无效[16]。有研究者分析油菜素内酯浸种对臭椿种子、豇豆种子萌发的影响发现,浸种后其种子发芽率、发芽势均提高,发芽速度缩短,根长和芽长、根干重和芽干重均增加,种子产量提高[17-18]。
目前,已有报道发现油菜素内酯在其他植物中有效促进了种子萌发,但尚未见油菜素内酯对谷子萌发影响机制方面的研究,因此研究油菜素内酯浸种对盐胁迫下谷子萌发的影响及其生理机制具有重大意义。本研究通过油菜素内酯浸种对盐胁迫谷子萌发的影响试验,以期找到最适的EBL浸种施用方式,为谷子在盐渍地上的高产种植提供理论依据和实践参考,从而促进我国农业的可持续发展。
1 材料与方法
1.1 试验地点与材料
试验于2024年2月在吕梁学院植物生理实验室进行,供试材料为晋谷21号,购买自山西鑫腾达农业科技有限公司。
1.2 试验方法
1.2.1 谷子挑选及浸种预处理
将无水乙醇稀释为75%的乙醇溶液,供谷子消毒使用。配制油菜素内酯母液,并稀释为10^-7、10^-8、10^-9、10^-10 mol/L浓度,供谷子浸种使用。称取NaCl,配制成50、100、150、200、250、300 mmol/L的NaCl溶液,供谷子盐胁迫使用。对晋谷21号的种子进行粗挑选,去掉干瘪的籽粒,将留下的谷子在75%乙醇中浸泡20s,用蒸馏水洗涤3次,再用吸水纸吸干谷子表面水分,分别使用配制好的不同浓度的油菜素内酯溶液浸种处理24h,依次表示为EBL1、EBL2、EBL3、EBL4,以蒸馏水浸种24h为对照组,表示为EBL0。
1.2.2 谷子萌发培养
在浸种处理24h后,将浸泡谷子的浸种液倒掉,将谷子置于滤纸上,在室内自然晾干。在直径为9cm的玻璃培养皿中放置双层滤纸,在处理好的培养皿中分别加入不同浓度的NaCl溶液,浓度分别为0(CK,蒸馏水)、50、100、150、200、250、300 mmol/L,每个试验设置3次重复。进一步挑选籽粒饱满、大小一致的谷子各100粒分别置于上述培养皿中,保持NaCl溶液始终浸没种子高度的一半。最后,将上述处理好的种子放置于人工气候箱中,于28℃黑暗条件下培养,培养期间始终保持滤纸湿润。谷子萌发后3d测定其发芽势,发芽后7d测定其发芽率,同时进行相关指标的计算。
1.3 指标的测定
1.3.1 发芽势、发芽率的测定
以根、芽长度均超过谷子直径的一半作为发芽标准,从发芽后2d开始每天记录种子发芽数,将发芽后3d的发芽数用于计算发芽势。基于发芽后7d的发芽数计算发芽率。发芽势=发芽后3d的发芽数/供试谷子粒数×100%;发芽率=发芽后7d的发芽数/供试谷子粒数×100%。
1.3.2 胚根、胚轴长度的测定
谷子发芽7d后,从每个培养皿中随机选取5粒萌发的谷子,用刚尺分别测量其胚根、胚轴长度,每个处理重复3次。结果取平均值。
1.3.3 萌发后含水量的测定
谷子萌发后7d,取每个处理浓度的谷子10粒,用吸水纸吸干种子表面残留水分,称取谷子鲜重(FW),在电热鼓风干燥箱中于105℃烘干至恒重,称得干重(DW)。萌发谷子含水量=[(FW-DW)/FW]×100%。每个处理重复3次,结果取平均值。
1.3.4 丙二醛(MDA)含量、抗氧化酶活性的测定
丙二醛含量用硫代巴比妥酸法测定;超氧化物歧化酶活性用氮蓝四唑还原法测定;过氧化物酶活性用愈创木酚比色法测定[19]。
试验过程中测得的各数据均用 Excel 2021、SPSS27.0进行处理、统计分析等操作,数据均表示为“平均数±标准差”格式,采用Duncan's新复极差测验法(α=0.05)进行单因素显著性方差分析。
2 结果与分析
2.1 不同处理对谷子萌发的调控效应
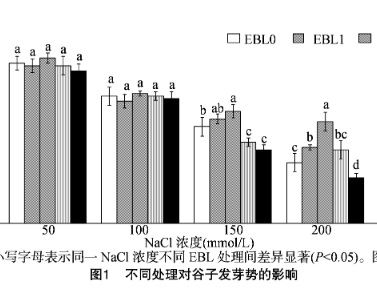
由图1可知,随着NaCl胁迫浓度的升高,每组EBL浸种处理均降低了谷子的发芽势。在无NaCl胁迫的条件下,EBL3浸种处理(即10^-8 mol/L EBL处理)的谷子发芽势较其他浓度EBL处理组高,但差异不显著。在50、100mmol/L NaCl胁迫下,EBL2浸种处理(即10^-9 mol/L EBL处理)的谷子发芽势比其他浓度EBL处理组高,但差异均不显著。在150 mmol/L NaCl胁迫下,与EBL0浸种处理相比,随EBL浸种浓度的上升,谷子发芽势首先表现为升高趋势,其中EBL2浸种处理(即10^-9 mol/L EBL处理)的发芽势达最高;随着EBL浸种浓度进一步上升,谷子发芽势降低;EBL0~EBL2浸种处理与EBL3、EBL4处理组相比,对谷子发芽势的促进效果达到显著水平(P<0.05)。在200mmol/L NaCl胁迫下,与EBL0浸种处理相比,EBL1~EBL3浸种处理(即10^-10~10^-8 mol/L EBL处理)谷子的发芽势均升高,EBL4浸种处理(即10^-7 mol/L EBL处理)的谷子发芽势降低;在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子发芽势达到最大值,且与其他EBL处理组间均有显著差异(P<0.05)。在250 mmol/L NaCl胁迫下,与EBL0浸种处理相比,随着EBL浸种浓度的上升,谷子的发芽势首先表现为升高趋势,其中EBL2浸种处理(即10^-9 mol/L EBL处理)的谷子发芽势达到最大值;随着EBL浸种浓度进一步升高,谷子的发芽势降低;在EBL0~EBL2浸种处理(即0、10^-10、10^-9 mol/L EBL处理)下,与EBL3、EBL4处理组相比,对谷子的发芽势均起到了促进效果。300 mmol/L NaCl胁迫下,各组EBL浸种处理均对谷子的发芽势无显著影响。
由图2可知,随着NaCl胁迫浓度的升高,各EBL浸种处理均降低了谷子的发芽率。在无NaCl胁迫处理下,EBL1浸种处理(即10^-10 mol/L EBL处理)的谷子发芽率高于其他EBL处理,但差异不显著。在50 mmol/L NaCl胁迫下,EBL2浸种处理(即10^-9 mol/L EBL处理)的谷子发芽率高于其他浓度EBL处理,但差异不显著。在100 mmol/L NaCl溶液处理下,各EBL浸种处理均对谷子发芽率无显著影响。在150 mmol/L NaCl胁迫下,EBL1~EBL3浸种处理(即10^-10~10^-8 mol/L EBL处理)的谷子发芽率高于其他处理;在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子的发芽率达到最大值;在EBL4浸种处理(即10^-7 mol/L EBL处理)下,谷子发芽率降低;EBL1~EBL3处理组与EBL4处理组相比,对谷子发芽率的促进效果均达到显著水平(P<0.05)。在200mmol/L NaCl胁迫下,与EBL0浸种处理相比,EBL1~EBL3浸种处理(即10^-10~10^-8 mol/L EBL处理)均可提高谷子的发芽率;在EBL4浸种处理(即10^-7 mol/L EBL处理)下,谷子发芽率较其他处理降低;在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子的发芽率达到最大值,且此处理与其他处理相比差异显著(P<0.05),谷子发芽率分别比EBL0、EBL1、EBL3、EBL4处理组提高32.76%、17.24%、12.07%和50.00%。在250 mmol/L NaCl胁迫下,与EBL0浸种处理相比,随EBL浸种浓度的上升,谷子发芽率升高,EBL1、EBL2浸种处理(即10^-10、10^-9 mol/L EBL处理)谷子发芽率较其他处理差异显著(P<0.05),但这2组处理间差异不显著;随着EBL浸种浓度继续上升,谷子发芽率降低,EBL3浸种处理(即10^-8 mol/L EBL处理)对谷子发芽率的抑制作用与EBL0处理相比差异不显著,EBL4浸种处理(即10^-7 mol/L EBL处理)较EBL0处理显著抑制了谷子发芽率(P<0.05)。在300mmol/L NaCl胁迫下,各EBL浸种处理均对谷子发芽率无显著影响。
2.2 不同处理对谷子胚根、胚轴长度的调控效应
由图3可知,随着NaCl胁迫浓度的升高,各EBL浸种处理整体上降低了谷子萌发期间的胚根长度。在无NaCl胁迫处理下,各EBL浸种处理对谷子萌发期间的胚根长度无显著影响。在50 mmol/L NaCl胁迫处理下,EBL2浸种处理(即10^-9 mol/L EBL处理)谷子萌发期间的胚根长度较其他EBL处理组高(除EBL0浸种处理外),但差异不显著。在100mmol/L NaCl胁迫下,EBL2浸种处理(即10^-9 mol/L EBL处理)谷子萌发期间的胚根长度大于其他EBL处理组,但差异不显著。在150 mmol/L NaCl胁迫下,与EBL0浸种处理相比,EBL1~EBL3浸种处理(即10^-10、10^-9、10^-8 mol/L EBL处理)均增加了谷子萌发期间的胚根长度;在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子胚根长度达到最大值;与其他处理相比,EBL4浸种处理(即10^-7 mol/L EBL处理)降低了谷子萌发期间的胚根长度。在200mmol/L NaCl胁迫下,与EBL0浸种处理相比,EBL1~EBL3浸种处理(即10^-10、10^-9、10^-8 mol/L EBL处理)均增加了谷子萌发期间的胚根长度;EBL4浸种处理(即10^-7 mol/L EBL处理)降低了谷子萌发期间的胚根长度;在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子的胚根长度达到最大值,且此处理组与除EBL3处理组以外的其他处理组相比均有显著差异(P<0.05)。在250mmol/L NaCl胁迫下,EBL2浸种处理(即10^-9 mol/L EBL处理)谷子萌发期间的胚根长度高于其他EBL处理组,与EBL4浸种处理(即10^-7 mol/L EBL处理)间差异显著(P<0.05)。在300 mmol/L NaCl胁迫下,EBL1、EBL2浸种处理(即10^-10、10^-9 mol/L EBL处理)谷子萌发期间的胚根长度大于其他EBL处理,与EBL4浸种处理(即10^-7 mol/L EBL处理)差异显著(P<0.05)。
由图4可知,随着NaCl胁迫浓度的升高,各EBL浸种处理整体上均降低了谷子萌发期间的胚轴长度。在无NaCl胁迫处理下,EBL3浸种处理(即10^-8 mol/L EBL处理)谷子萌发期间的胚轴长度大于其他EBL处理,但差异不显著。在50 mmol/L NaCl胁迫下,EBL2浸种处理(即10^-9 mol/L EBL处理)谷子萌发期间的胚轴长度大于其他EBL处理,但差异不显著。在100 mmol/L NaCl胁迫下,EBL2、EBL3浸种处理(即10^-9、10^-8 mol/L EBL处理)谷子萌发期间的胚轴长度大于其他EBL处理,但差异不显著。在150、200 mmol/L NaCl胁迫处理下,与EBL0浸种处理相比,EBL1~EBL3浸种处理(即10^-10、10^-9、10^-8 mol/L EBL处理)谷子萌发期间的胚轴长度均增加,EBL4浸种处理(即10^-7 mol/L EBL处理)谷子萌发期间的胚轴长度均降低;在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子胚轴长度均达到最大值,且各EBL浸种处理对谷子萌发期间的胚轴长度有不同程度的影响。在250mmol/L NaCl胁迫处理下,各EBL浸种处理对谷子萌发期间的胚轴长度无显著影响。在300 mmol/L NaCl胁迫下,EBL1浸种处理(即10^-10 mol/L EBL处理)谷子萌发期间的胚轴长度较其他EBL处理组显著增加(P<0.05)。
由图3、图4可知,在同一NaCl浓度胁迫下,随着EBL浸种浓度的上升,谷子萌发期间胚根和胚轴长度均先上升后下降,且胚根长度的降低幅度比胚轴长度更明显,即胚根比胚轴对盐胁迫下EBL处理更敏感。
2.3 不同处理组对谷子萌发后含水量的调控效应
由图5可知,随着NaCl胁迫浓度的升高,各EBL浸种处理整体上均降低了谷子萌发后的含水量。在0、50 mmol/L NaCl胁迫处理下,与EBL0浸种处理谷子萌发后的含水量最低,但不同处理间的差异不显著;在EBL3浸种处理(10^-8 mol/L EBL处理)下,萌发后含水量达到最大值。在100 mmol/L NaCl胁迫下,与EBL0浸种处理相比,EBL2浸种处理(即10^-9 mol/L EBL处理)谷子萌发后的含水量提高,但变化不显著。在150 mmol/L NaCl胁迫处理下,与EBL0浸种处理相比,EBL1~EBL3处理(即10^-10、10^-9、10^-8 mol/L EBL浸种处理)均增加了谷子萌发后的含水量,EBL4浸种处理(即10^-7 mol/L EBL处理)降低了谷子萌发后的含水量,其中在EBL2浸种处理(即10^-9 mol/L EBL处理)下,谷子萌发后的含水量达到最大值,并且此处理组与除EBL3外的其他处理组相比差异显著(P<0.05)。在200 mmol/L NaCl胁迫下,与EBL0浸种处理相比,EBL1~EBL3浸种处理(10^-10~10^-8 mol/L EBL处理)谷子萌发后的含水量均增加,EBL4浸种处理(即10^-7 mol/L EBL处理)谷子萌发后的含水量较其他处理降低,其中EBL2浸种处理(即10^-9 mol/L EBL处理)下的含水量达到最大值,且此处理与其他处理间的差异均显著(P<0.05)。在250、300mmol/L NaCl胁迫下,EBL2浸种处理(即10^-9 mol/L EBL处理)谷子萌发后含水量整体上高于其他浓度EBL处理,但差异不显著。
对以上试验测得的谷子发芽势、发芽率、萌发期间胚根长度、胚轴长度、萌发后的含水量等5个指标进行综合分析,结果显示,EBL2浸种处理(即10^-9 mol/L EBL处理)对200mmol/L NaCl胁迫下谷子萌发的影响最显著。
2.4 最佳处理对谷子丙二醛含量、抗氧化酶活性的影响
由图6可知,NaCl胁迫处理下谷子萌发后的MDA含量(以谷子萌发后的鲜重为基础计算,下同)表现出显著增加的趋势;与NaCl胁迫处理相比,在NaCl胁迫条件下用EBL2浸种的谷子MDA含量降低,差异达到显著水平(P<0.05)。
由图7、图8可知,与对照组相比,EBL2浸种处理的萌发谷子的POD活性显著上升(P<0.05),而SOD活性差异不显著。在NaCl胁迫下,萌发谷子的2种酶活性均显著上升;与NaCl胁迫相比,在NaCl胁迫条件下施用EBL2浸种处理的谷子SOD、POD活性均呈现显著上升的趋势(P<0.05)。
3 结论与讨论
本试验过程中,不同浓度的NaCl胁迫均不同程度地抑制谷子的萌发效果,通过在NaCl胁迫前进行不同浓度的EBL浸种处理,对谷子萌发的影响呈现不同变化。在0、50、100mmol/L等低浓度NaCl胁迫下,施用不同浓度的EBL对谷子的发芽势、发芽率、萌发期间胚根长度、胚轴长度、萌发后的含水量5个指标整体有一定的增加,但增加趋势均不显著;在150、200 mmol/L等中等浓度NaCl胁迫下,施用不同浓度的EBL对谷子萌发情况呈现不同程度的影响。综合分析可知,10^-9 mol/L EBL浸种处理对200 mmol/L NaCl胁迫下谷子萌发的促进效果最好;250 mmol/L高浓度NaCl胁迫下,施用不同浓度的EBL对谷子发芽势、发芽率的影响有一定的差异,但对谷子萌发期间的胚轴长度以及萌发后的含水量均无显著差异;在300mmol/L极高浓度NaCl胁迫下,施用不同浓度的EBL对谷子萌发情况影响均不大。对试验所得的促进谷子萌发效果最好的NaCl浓度、EBL浸种浓度单独作用于谷子,测定其丙二醛含量、超氧化物歧化酶和过氧化物酶活性,得出NaCl胁迫下,MDA含量较高,超氧化物歧化酶、过氧化物酶活性较低,而用EBL浸种处理后,MDA含量会降低,相应的抗氧化物酶活性会升高。
范翠枝等做了不同浓度的油菜素内酯浸种对不同浓度的NaCl胁迫番茄种子萌发的试验,测定了番茄种子萌发期相应抗氧化代谢指标,结果表明,10^-9 mol/L EBL浸种对150 mmol/L NaCl胁迫下的番茄种子萌发效果最好,促进了SOD、POD活性的上升[20]。本试验结果与上述研究结果[20]一致,本试验结果得出的最适NaCl胁迫浓度与上述研究结果不一致,是由于不同物种对盐的耐受性不同,谷子是耐盐作物,耐盐浓度比番茄高。赵旭庆等研究了不同NaCl胁迫、不同油菜素内酯浸种对盐溶液处理下黑果枸杞种子萌发的影响,发现低浓度的NaCl能促进种子的萌发,高浓度处理则会抑制种子萌发;适宜浓度EBL浸种能促进种子萌发,但浓度过高时可能会有抑制作用;0.05mg/L EBL对促进其种子萌发效果最明显[21]。本试验结果与上述研究结果存在不一致的地方,本试验得出,低浓度的NaCl对谷子萌发没有表现出显著的促进或抑制效应,可能是由于不同物种对低浓度NaCl胁迫的反应不同或配制的NaCl溶液浓度不同导致结论不同,具体的原因值得后续进一步研究。
参考文献:
[1] Yue J M, Fu Z Y, Zhang L, et al. The positive effect of different 24-epiBL pretreatments on salinity tolerance in Robinia pseudoacacia L. seedlings[J]. Forests, 2019, 10(1): 4.
[2] 吴双. 谷子栽培及病虫害防治技术[J]. 现代农村科技, 2024(4): 49-50.
[3] 张笛, 苗兴芬, 王雨婷. 100份谷子品种资源萌发期耐盐性评价及耐盐品种筛选[J]. 作物杂志, 2019(6): 43-49.
[4] Diao X M. Production and genetic improvement of minor cereals in China[J]. The Crop Journal, 2017, 5(2): 103-114.
[5] Zeng P, Zhu P W, Qian L F, et al. Identification and fine mapping of qGR6.2, a novel locus controlling rice seed germination under salt stress[J]. BMC Plant Biology, 2021, 21(1): 36.
[6] 陈晨, 程大伟, 李兰, 等. 油菜素内酯调控植物耐盐机理研究进展[J]. 中国农业科技导报, 2024, 26(2): 1-12.
[7] 郑婷, 程建徽, 魏灵珠, 等. 油菜素内酯及其在园艺植物中的研究进展[J/OL]. 分子植物育种, 2024: 1-9[2024-04-15]. http://kns.cnki.net/kcms/detail/46.1068.s.20220113.1105.004.html.
[8] 权梦萍, 徐佳慧, 尹佳茗, 等. 油菜素内酯调控植物响应非生物逆境胁迫的生理机制[J]. 植物保护学报, 2023, 50(1): 22-31.
[9] 王丹, 刘亚西, 周扬, 等. 油菜素内酯对盐胁迫下黑麦草种子萌发及幼苗生长的生理调控作用[J]. 草业科学, 2021, 38(6): 1110-1118.
[10] 侯会云. 油菜素内酯对盐胁迫下水稻种子萌发的影响[J]. 热带农业科学, 2020, 40(7): 1-6.
[11] Semida W M, Rady M M. Pre-soaking in 24-epibrassinolide or salicylic acid improves seed germination, seedling growth, and anti-oxidant capacity in Phaseolus vulgaris L. grown under NaCl stress[J]. The Journal of Horticultural Science and Biotechnology, 2014, 89(3): 338-344.
[12] Rathinavelu S. Impact of plant growth regulators and nutrient consortium on growth, superoxide dismutase, Na+/K+ ratio and yield of blackgram under salinity stress[J]. International Journal of Agriculture, Environment and Biotechnology, 2018, 11(5): 791-798.
[13] 吕宗环, 韩康妮, 杜晓芬, 等. 谷子萌发期耐盐种质鉴定及应用[J]. 植物科学学报, 2024, 42(1): 75-84.
[14] 张永芳, 宋喜娥, 王润梅, 等. Na2CO3胁迫对谷子种子萌发的影响[J]. 种子, 2015, 34(11): 94-97.
[15] Nie W J, Gong B, Geng B, et al. The effects of exogenous 2,4-epibrassinolide on the germination of cucumber seeds under NaHCO3 stress[J]. Plants, 2024, 13(3): 394.
[16] Chakma S P, Chileshe S M, Thomas R, et al. Cotton seed priming with brassinosteroid promotes germination and seedling growth[J]. Agronomy, 2021, 11(3): 566.
[17] Li K R, Zhang W B, Li H K. Effect of natural brassinolide on germination of Ailanthus altissima seeds[J]. Forestry Studies in China, 2005, 7(2): 12-14.
[18] Fariduddin Q, Hayat S, Ali B, et al. Effect of 2,8-homobrassinolide on the growth and yield of vigna[J]. Annals of Agri-Bio Research, 2005, 21(1): 1-6.
[19] 高俊凤. 植物生理学实验指导[M]. 北京: 高等教育出版社, 2006: 210-217.
[20] 范翠枝, 吴馨怡, 关欣, 等. 油菜素内酯浸种对盐胁迫番茄种子萌发的影响及其生理机制[J]. 生态学报, 2021, 41(5): 1857-1867.
[21] 赵旭庆, 徐珊珊, 李强, 等. 盐胁迫下24-表油菜素内酯浸种对黑果枸杞种子萌发的影响[J]. 林业科技通讯, 2021(3): 59-61.





